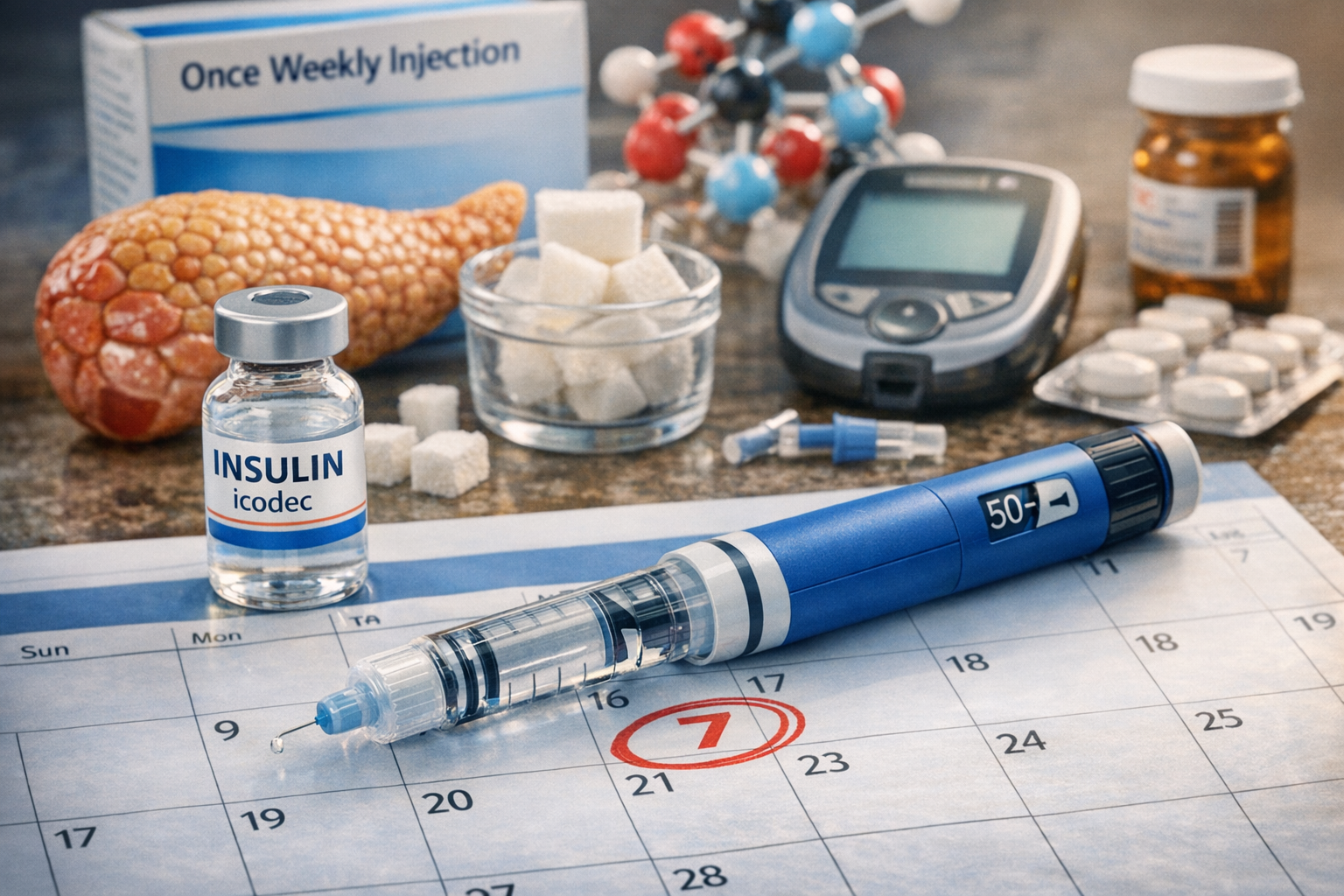
A aprovação da insulina icodeca-abae (Awiqli®, Novo Nordisk) pela Food and Drug Administration (FDA) marca uma mudança potencialmente relevante no tratamento do diabetes tipo 2. Pela primeira vez, pacientes adultos passam a contar com uma insulina basal de aplicação semanal, substituindo o regime tradicional de uma injeção diária.
A nova formulação foi aprovada como adjuvante à dieta e ao exercício para adultos com diabetes tipo 2 e representa a primeira classe inédita de insulina basal aprovada nos Estados Unidos em mais de duas décadas. A expectativa é de que a estratégia reduza uma das principais barreiras ao início e à manutenção da insulinoterapia: a necessidade de aplicações diárias.
Menos Injeções, Mesma Eficácia
A Awiqli® utiliza a molécula insulina icodeca-abae, uma insulina basal de ação ultraprolongada formulada para ser aplicada apenas uma vez por semana, sempre no mesmo dia. Na prática, isso reduz o número de injeções de sete para uma a cada período de sete dias.
A aprovação foi baseada no programa clínico fase 3a ONWARDS, composto por quatro estudos randomizados envolvendo aproximadamente 2.680 adultos com diabetes tipo 2 não controlado. Os estudos compararam a insulina semanal com insulinas basais diárias, como degludeca e glargina. Em todos os estudos, a icodeca demonstrou redução significativa da hemoglobina glicada (HbA1c), com eficácia comparável — e em alguns cenários superior — às terapias diárias.
No estudo ONWARDS 3, realizado em pacientes que nunca haviam utilizado insulina, a redução média de HbA1c foi de 1,6% com a insulina semanal, em comparação com 1,4% com a insulina glargina diária. Além disso, os pacientes tratados com a formulação semanal permaneceram mais tempo dentro da faixa glicêmica-alvo.
Possível Impacto Sobre Adesão ao Tratamento
A adesão à insulinoterapia continua sendo um dos principais desafios no diabetes tipo 2. Muitos pacientes atrasam o início da insulina ou apresentam baixa adesão devido ao desconforto com aplicações frequentes, medo de hipoglicemia e complexidade do regime terapêutico.
Especialistas envolvidos no desenvolvimento da icodeca acreditam que o esquema semanal pode facilitar a adesão e reduzir falhas de tratamento. Dados prévios sugerem que parte dos pacientes em uso de insulina basal deixa de aplicar até três ou quatro doses por semana. Nesse contexto, uma aplicação semanal poderia simplificar significativamente a rotina terapêutica.
Julio Rosenstock, investigador principal do programa ONWARDS, afirmou que a disponibilidade de uma insulina semanal pode “redefinir o manejo da insulina” em pacientes com diabetes tipo 2, sobretudo naqueles que apresentam resistência ao início da terapia basal.
Hipoglicemia Continua Sendo Ponto de Atenção
Apesar dos resultados positivos, a aprovação também veio acompanhada de alertas. A hipoglicemia permanece o evento adverso mais frequente, e alguns estudos demonstraram taxas numericamente maiores de hipoglicemia nível 2 ou 3 com a insulina semanal em comparação à insulina degludeca.
Como a medicação possui duração prolongada, erros de dose ou aplicações inadequadas podem ter consequências mais duradouras. Por isso, a bula recomenda monitorização glicêmica mais próxima, especialmente durante a transição de uma insulina basal diária para o esquema semanal.
A Awiqli® está contraindicada em episódios de hipoglicemia e em pacientes com hipersensibilidade à insulina icodeca ou a qualquer componente da formulação. Também é recomendado cuidado adicional em pacientes com doença renal, insuficiência hepática, insuficiência cardíaca, gestação ou uso concomitante de tiazolidinedionas.
Quando a Nova Opção Pode Ser Mais Útil
A principal população potencialmente beneficiada inclui pacientes com diabetes tipo 2 que adiam o início da insulina, apresentam dificuldade em manter a aplicação diária ou têm baixa adesão ao tratamento. A nova formulação também pode ser uma alternativa interessante em pacientes que já utilizam múltiplas medicações semanais, como agonistas de GLP-1.
Por outro lado, a insulina semanal ainda não foi aprovada para diabetes tipo 1, crianças ou adolescentes. Em 2024, a FDA chegou a recusar temporariamente a indicação para diabetes tipo 1 devido a preocupações relacionadas ao risco de hipoglicemia grave e a questões de fabricação.
Perspectiva
A chegada da primeira insulina basal semanal representa uma das mudanças mais relevantes no tratamento do diabetes tipo 2 nos últimos anos. Embora ainda sejam necessários dados de vida real e experiência clínica após o lançamento, a nova estratégia tem potencial para melhorar a adesão, simplificar o tratamento e ampliar o acesso à insulinoterapia em pacientes que hoje permanecem sem controle glicêmico adequado.
Referências
- FDA approves first once-weekly insulin for type 2 diabetes. Medscape. 2026 Mar 30. Disponível em: https://www.medscape.com/viewarticle/fda-approves-first-once-weekly-insulin-type-2-diabetes-2026a10009mv
- Lingvay I, Asong M, Desouza C, et al. Once-weekly insulin icodec vs once-daily insulin degludec in adults with insulin-naive type 2 diabetes: the ONWARDS 3 randomized clinical trial. JAMA. 2023;330(3):228-237. doi:10.1001/jama.2023.11313.
- FDA approves insulin icodec-abae, first once-weekly basal insulin for adults with T2D. Pharmacy Times. 2026 Mar 27.
- FDA approves novel weekly basal insulin for T2D. Am J Manag Care. 2026 Apr 2.
- FDA approves once-weekly basal insulin Awiqli for type 2. diaTribe. 2026 Mar 28.